美FDA发布严厉的COVID-19血清学检测警告
导读:美国食品药品监督管理局(FDA)已警告COVID-19血清学检测制造商不要夸大其产品的有用性或声称获得联邦批准,并警告说,这种诊断方法的意义可能还为时过早。
据外媒SlashGear报道,美国食品药品监督管理局(FDA)已警告COVID-19血清学检测制造商不要夸大其产品的有用性或声称获得联邦批准,并警告说,这种诊断方法的意义可能还为时过早。与更广泛的测试过程不同,血清学测试是在患者的样本中寻找新冠病毒本身,而不是寻找身体对感染的免疫反应。
这是一个重要的区别,尽管很多人似乎都会混淆这一点。例如,通过检测病毒本身是否存在,可以看出患者目前是否感染了COVID-19。
然而,通过寻找免疫反应---具体来说,就是抗体或血液中存在的蛋白质,当身体对感染作出反应时,就会出现抗体或蛋白质--你可以潜在地知道患者是否感染了新冠病毒,即使他们目前没有被感染。这对于评估人群,看看COVID-19的传播程度,以及看看有多少人可能对未来的感染有免疫力,这一点很重要。
"在感染的早期,当身体的免疫反应仍在建立时,抗体可能无法被检测到,"FDA解释说。"这限制了该检测对诊断COVID-19的有效性,以及为什么不应作为诊断COVID-19的唯一依据。"
COVID-19血清学检测很重要,但不是一蹴而就的
这个时效性的问题是大范围的检测不能仅仅依靠血清学方法的原因。目前,FDA已经在紧急使用授权(EUA)程序下对单一的血清学检测进行了授权,允许在新冠病毒大流行期间尽早应用药物和检测流程。这就是Cellex公司的qSARS-CoV-2 IgG/IgM快速检测试剂盒获得授权的原因,该试剂盒的设计是由批准的实验室使用。
显然,还有70多家测试开发商已经通知FDA,他们有血清学诊断方法可供使用。不过眼下,他们还没有获得授权,没有一家能够声称获得该机构的批准。"但是,一些公司谎称他们的血清学检测项目获得了FDA的批准或授权,或者谎称他们可以诊断出COVID-19,"FDA表示。"FDA将对虚假宣称或营销不准确可靠的检测项目的公司采取适当的行动。"
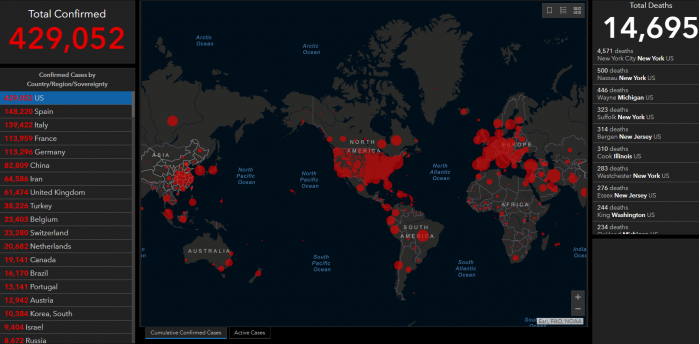
如果没有一致的COVID-19测试,就很难评估其反应
目前,美国至少有42个州发布了某种 “居家令”。据信美国约有95%的人口受到其中一项命令的影响,尽管有几个州继续拒绝颁布这些措施。立法者面临的挑战是了解这些努力如何影响COVID-19的进展。如果没有一致的、广泛的测试,实际上不可能确定新冠病毒对人群的影响程度。相反,只有死亡率数字作为决策的依据。
截至发稿前,美国新冠病毒确诊病例已达429052例,死亡病例达14695例。这不仅包括50个州,还包括哥伦比亚特区、波多黎各、关岛、北马里亚纳群岛和美属维尔京群岛。